ЭЛЕКТРОЛИЗЕРЫ МБ
| Электролизер | МБ 1,56 | МБ 3,2 | МБ 6,25 | МБ 12,5 А+К+Б | МБ 12,5 А+К | МБ 25 | МБ 50 | МБ 75 | МБ 100 | МБ 125 | МБ 150 |
| Производительностьэлектролизера по хлору, кг /сут | 1,56 | 3,2 | 6,25 | 12,5 | 12,5 | 25 | 50 | 75 | 100 | 125 | 150 |
| Размеры ячейки (наружные), мм | 350 х 215 | 350 х 320 | 350 х 600 | 350 х 600 | 615 х 675 | 615 х 1200 | 615 х 1200 | 615 х 1200 | 615 х 1200 | 615 х 1200 | 615 х 1200 |
| Рабочая поверхность ячейки (внутренняя) | 0,04 | 0,08 | 0,16 | 0,16 | 0,34 | 0,63 | 0,63 | 0,63 | 0,63 | 0,63 | 0,63 |
| Число разрядных промежутков | 1 | 1 | 1 | 2 | 1 | 1 | 2 | 3 | 4 | 5 | 6 |
| Нагрузка расчетная, кА | 57,93 | 118,84 | 232,10 | 232,10 | 464,20 | 928,40 | 928,40 | 928,40 | 928,40 | 928,40 | 928,40 |
| Плотность тока, кА/м2 | 1,60 | – | – | – | – | – | – | – | – | – | – |
| Нагрузка линейная,кА | 0,06 | 0,13 | 0,26 | 0,26 | >0,54 | 1,00 | 1,00 | 1,00 | 1,00 | 1,00 | 1,00 |
| Напряжение на ячейке, В | 5 | 5 | 5 | 5 | 5 | 5 | 5 | 5 | 5 | 5 | 5 |
| Напряжение на электролизере, В | 5 | 5 | 5 | 10 | 5 | 5 | 10 | 15 | 20 | 35 | 30 |
| Температура электролиза,не более°С | 60 | – | – | – | – | – | – | – | – | – | – |
| Производительность кг/час: | |||||||||||
| хлор | 0,065 | 0,134 | 0,261 | 0,522 | 0,522 | 1,044 | 2,088 | 3,132 | 4,176 | 5,220 | 6,264 |
| гидроксид натрия | 0,073 | 0,151 | 0,294 | 0,588 | 0,588 | 1,176 | 2,352 | 3,527 | 4,703 | 5,879 | 7,055 |
| водород | 0,002 | 0,004 | 0,009 | 0,017 | 0,017 | 0,034 | 0,069 | 0,103 | 0,137 | 0,172 | 0,206 |
| Габариты, мм : | – | – | – | – | – | – | – | – | – | – | – |
| длина L | 545 | 565 | 565 | 690 | 590 | 1135 | 1205 | 1285 | 1355 | 1435 | 1505 |
| ширина B | 750 | 890 | 890 | 1000 | 1280 | 1350 | 1350 | 1350 | 1440 | 1440 | 1440 |
| высота Н | 1630 | 2240 | 2240 | 2330 | 2330 | 3025 | 3025 | 3025 | 3240 | 3240 | 3240 |
Выход по току: хлор 85%, водород 100%, щелочь 85%
Электролиз расплавов
При электролизе расплава на аноде окисляются анионы кислотных остатков, а на катоде восстанавливаются катионы металлов. Молекул воды в системе нет.
Например: электролиз расплава хлорида натрия. На катоде восстанавли-ваются катионы натрия:
Катод (–): Na+ + ē → Na
На аноде окисляются анионы хлора:
Анод (+): 2Cl– – 2ē → Cl2
Суммарное уравнение электролиза расплава хлорида натрия:
2Na+Cl– → 2Na + Cl2
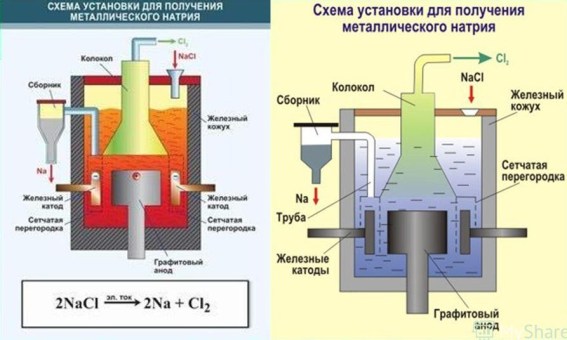
Еще один пример: электролиз расплава гидроксида натрия. На катоде восстанавливаются катионы натрия:
Катод (–): Na+ + ē → Na
На аноде окисляются гидроксид-ионы:
Анод (+): 4OH– – 4ē → O2 + 2H2O
Суммарное уравнение электролиза расплава гидроксида натрия:
4Na+OH– → 4Na + O2+ 2H2O
Многие металлы получают в промышленности электролизом расплавов.
Например, алюминий получают электролизом раствора оксида алюминия в расплаве криолита. Криолит – Na3[AlF6] плавится при более низкой температуре (1100оС), чем оксид алюминия (2050оС). А оксид алюминия отлично растворяется в расплавленном криолите.
В растворе криолите оксид алюминия диссоциирует на ионы:
Al2O3 = Al3+ + AlO33-
На катоде восстанавливаются катионы алюминия:
Катод (–): Al3+ + 3ē → Al
На аноде окисляются алюминат-ионы:
Анод (+): 4AlO33– – 12ē → 2Al2O3 + 3O2
Общее уравнение электролиза раствора оксида алюминия в расплаве криолита:
2Al2О3 = 4Al + 3О2
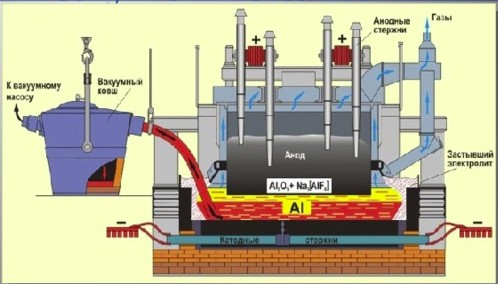
В промышленности при электролизе оксида алюминия в качестве электродов используют графитовые стержни. При этом электроды частично окисляются (сгорают) в выделяющемся кислороде:
C + О2 = C+4O2-2
Суть процесса
Движущей силой электролиза является электричество. Под действием энергии электрического тока осуществляется химическая реакция, которая не происходит самопроизвольно.
Процессы восстановления и окисления протекают раздельно, на различных электродах. В качестве электродов берутся любые материалы, способные проводить электрический ток. Чаще всего это металлы. Из неметаллов используют углерод, из него изготавливают графитовые стержни. В редких случаях в качестве электрода выступают жидкости.
В расплав помещают два противоположно заряженных электрода, к которым движутся разнозаряженные ионы.
Положительно заряженные катионы, в которых количество электронов меньше количества протонов, движутся к отрицательному полюсу электрода – катоду. В качестве катода берут металлическую пластину из меди, латуни, цинка, алюминия.
К аноду – положительному полюсу – движутся анионы. Это отрицательно заряженные ионы, в которых число электронов превышает количество протонов. Анод в процессе электролиза окисляется, то есть растворяется. Поэтому в качестве анода берут материал, не влияющий на химический процесс. Такой анод называется инертным электродом. Подходящие материалы – графит, платина.
Рис. 1. Движение анионов и катионов при электролизе.
Электролиз растворов протекает сложнее, чем расплавов. В растворе участвуют ионы вещества и ионы растворителя, в расплавах – только ионы вещества. Главным продуктом электролиза расплава является металл (всегда катион). Побочные продукты:
- газ – кислород, водород, хлор;
- жидкости – вода, оксид серы (VI), бром.
Рис. 2. Схема установки для получения натрия электролизом.
На катоде происходит процесс восстановления, на аноде – процесс окисления.
Что такое электролизер
Электролизер – это специальная установка, применяемая для выделения из раствора или расплава его составляющих.
Основными характеристиками электролизера являются:
- Рабочее напряжение для одного электрода колеблется в интервале от 1,8 до 2,0 В;
- Сила тока – для нормального протекания процесса электролиза на электроды подают ток с значением данной характеристики от 5 до 10 А;
- Количество электродов – минимальное количество электродов – 2, максимальное ограничивается размерами самой установки и ее предназначением;
- Габариты электродов – в качестве электродов используют не угольные стержни, а металлические пластины, размер которых определяется предназначением установки, вольт-амперной характеристикой подаваемого на пластины тока;
- Расстояние между разноименно заряженными поверхностями электродов – минимальное расстояние между пластинами-электродами должно быть не менее 1,5 мм;
- Материал электрода – в современных электролизерах в качестве материала для анода и катода используют листовую нержавеющую сталь с добавкой никеля.
Также еще одной важной характеристикой электролизной установки является использование катализаторов. Применяются такие установки для следующих целей:
Применяются такие установки для следующих целей:
- Получение гремучего газа, состоящего из смеси водорода и кислорода (газ Брауна);
- Выделение чистого алюминия, магния, цинка из расплавов их солей;
- Очистка воды от растворенных в ней солей и примесей;
- Нанесение на поверхность металлических деталей тонкого препятствующего коррозии слоя никеля, цинка;
- Обеззараживание пищевых продуктов;
- Очистка сточных вод от растворенных в них солей тяжелых металлов и других вредных веществ.
Важно! Платина-электрод из обычного железа применяется в электролизных установках реже, чем из нержавейки, так как оно быстрее окисляется и приходит в негодность
О нас
Наше предприятие выполняет полный спектр ремонтных и сервисных работ водородных станций и электролизеров, в наличии всегда имеются все необходимые запасные части и материалы. За 15 лет успешной работы выполнено более 400 проектов на территории РФ, а также в странах ближайшего зарубежья. Нашими клиентами являются крупнейшие заводы корпорации РосТех, генерирующие компании, металлургические заводы, а также предприятия химической и пищевой промышленности. Наша компания является производителем сертифицированных запчастей и расходных материалов для электролизных и водородных станций.
Виды электролизеров
Кратко ознакомимся с конструктивными особенностями основных видов устройств для расщепления воды.
Сухие
Конструкция прибора данного типа была показана на рисунке 2, ее особенность заключается в том, что манипулируя количеством ячеек, можно запитать устройство от источника с напряжением, существенно превышающим минимальный электродный потенциал.
Проточные
С упрощенным устройством приборов этого вида можно ознакомиться на рисунке 5. Как видим, конструкция включает в себя ванну с электродами «A», полностью залитую раствором и бак «D».
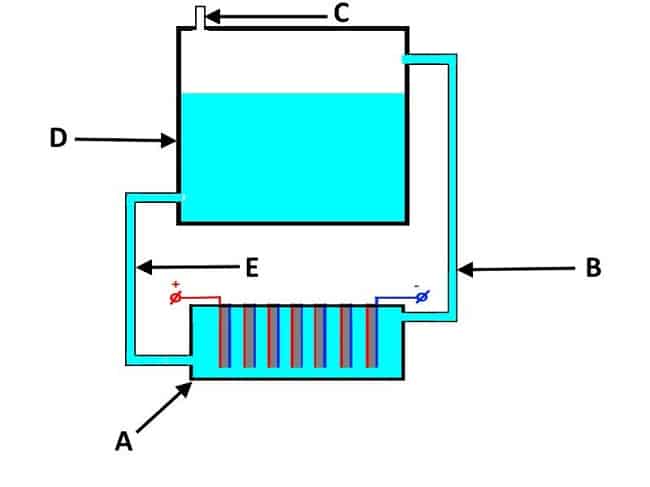 Рис 5. Конструкция проточного электролизера
Рис 5. Конструкция проточного электролизера
Принцип работы устройства следующий:
- входе электрохимического процесса газ вместе с электролитом выдавливается в емкость «D» через трубу «В»;
- в баке «D» происходит отделение от электролитного раствора газа, который выводится через выходной клапан «С»;
- электролит возвращается в гидролизную ванну через трубу «Е».
Мембранные
Основная особенность устройств этого типа – использование твердого электролита (мембраны) на полимерной основе. С конструкцией приборов этого вида можно ознакомиться на рисунке 6.
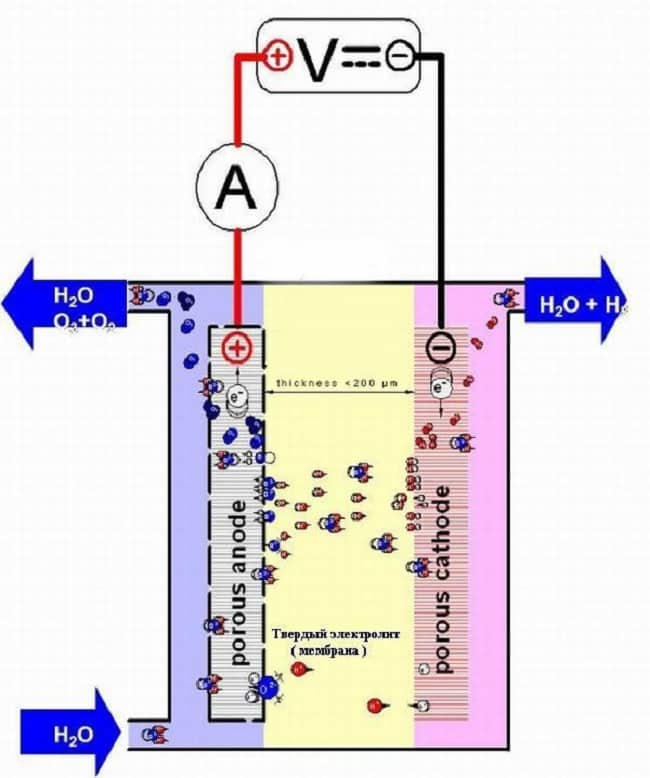 Рис 6. Электролизер мембранного типа
Рис 6. Электролизер мембранного типа
Основная особенность таких устройств заключается в двойном назначении мембраны, она не только переносит протоны и ионы, а и на физическом уровне разделяет как электроды, так и продукты электрохимического процесса.
Диафрагменные
В тех случаях, когда не допустима диффузия продуктов электролиза между электродными камерами, используют пористую диафрагму (что и дало название таким приборам). Материалом для нее может служить керамика, асбест или стекло. В некоторых случаях для создания такой диафрагмы можно использовать полимерные волокна или стеклянную вату. На рисунке 7 показан простейший вариант диафрагменного прибора для электрохимических процессов.
 Конструкция диафрагменного электролизера
Конструкция диафрагменного электролизера
Пояснение:
- Выход для кислорода.
- U-образная колба.
- Выход для водорода.
- Анод.
- Катод.
- Диафрагма.
Щелочные
Электрохимический процесс невозможен в дистиллированной воде, в качестве катализатора применяется концентрированный раствор щелочи (использование соли нежелательно, так как при этом выделяется хлор). Исходя из этого, щелочными можно назвать большую часть электрохимических устройств для расщепления воды.
На тематических форумах советуют использовать гидроксид натрия (NaOH), который, в отличие от пищевой соды (NaHCO3), не разъедает электрод. Заметим, что у последней имеются два весомых преимущества:
- Можно использовать железные электроды.
- Не выделяются вредные вещества.
Но, один существенный недостаток сводит на нет все преимущества пищевой соды, как катализатора. Ее концентрация в воде не более 80 грамм на литр. Это снижает морозостойкость электролита и его проводимость тока. Если с первым еще можно смириться в теплое время года, то второе требует увеличения площади пластин электродов, что в свою очередь, увеличивает размер конструкции.
Общее положение
Одним из важнейших элементов технологического процесса на промышленных предприятиях является применение газообразного чистого водорода. Процесс получения такого водорода осуществляется на основе использования водородных установок – электролизеров, технологически сложных и особо опасных в эксплуатационном плане объектов, требующих к себе повышенного внимания. В Российской Федерации электролитический водород широко применяется в различных отраслях экономики:
-
- в пищевой промышленности в основном для гидрогенизации жиров. Промышленность ориентирована на крупные блоки по 250 нм3Н2/ч, при этом отмечается возрастание вклада себестоимости водорода в отпускную цену продукта;
- в металлургии:
а) для получения металлов методом прямого восстановления руды (электролизеры ФВ-500);
б) для получения твердых сплавов (электролизерами СЭУ-40, в среднем 5–10 штук электролизеров на каждом заводе); - в электронной промышленности водород используется для создания восстановительной атмосферы. Одним из основных требований предприятий электронной промышленности к используемому водороду является его высокая чистота. Например, в некоторых процессах эпитаксии содержание примесей воды должно находиться на уровне не выше 0,01 ppm, что соответствует точке росы – 100ºС. Этим требованиям наилучшим образом соответствует водород, получаемый электролизом с последующей очисткой. Производство электролитического водорода на предприятиях электронной промышленности составляет заметную долю в его общем балансе.
- в энергетике водород используется для охлаждения мощных турбогенераторов благодаря его высокой теплопроводности и коэффициенту диффузии, а также нетоксичности. Для этой цели на крупных ТЭЦ и АЭС создаются электролизные станции с расходом водорода около 6,10-3м3/МВт∙ч. Таким образом, станция содержит 2 электролизера (один резервный) производительностью 10 или 20 нм3Н2/ч;
- в стекольной промышленности, где самым большим потребителем электролитического водорода (две станции – по 500 нм3Н2/час каждая на базе электролизеров СЭУ-40) является стекольный завод в г. Бор Нижегородской области. Данное предприятие традиционно обеспечивает стеклами отечественные автомобили, самолеты, при этом постоянно расширяя свой ассортимент;
- на предприятиях, производящих жидкий водород, современные потребности в котором составляют около 2 тыс. т. в год;
- у многих мелких потребителей водорода в фармацевтической, металлообрабатывающей и других отраслях;
- предприятия г. Зеленограда – не менее 1000 нм3 Н2/час;
- подольский химико-металлургический комбинат – 2000нм3 Н2/час;
- остальные – не менее 1000 нм3 Н2/час;
В близкой перспективе необходимость увеличения производства электролитического водорода будет обусловлена как развитием его традиционных потребителей, так и появлением новых, таких как автотранспорт, космонавтика, энергоустановки на основе топливных элементов, энергоустановки и
системы преобразования и аккумулирования энергии на базе возобновляемых энергоресурсов и многих других.



Описание
УЭ ГПХН 300Сe– электролизная установка проточного типа с производительностью 300 г в час по активному хлору или 7 кг акх в сутки. Электролизер расположен в квадратной трубе из полипропилена. Аноды – покрытие смешанные оксиды платиновой группы. электролизер – самоочищающийся (реверс). Установка комплектуется насосами фирмы «Этатрон» на подачу солевого раствора, подачу гипохлорита натрия в резервуары чистой воды. Трубы и фитинги, емкостное оборудование – полипропилен, стойкий к растворам гипохлорита. Клапаны – мембранные (не засаливаются гипохлоритом в процессе эксплуатации). Эффективность установки по преобразовании соли в хлор – до 99%.
Область применения
На станциях водоподготовки для обеззараживания поверхностных вод, подземных вод, очищенных сточных вод, плавательных бассейнов, птицефабрик, животноводческих комплексов, для отбеливания бумаги, в химической, фармацевтической промышленности, для производства дезинфицирующих и отбеливающих средств и т.д. При помощи УЭ ГПХН 300Се можно продезинфицировать бассейн объемом до 1200 куб.м или обеззаразить до 2400 куб.м. воды на станциях водоподготовки
Использование
УЭ ГПХН 300С – поставляется как на раме, так и для крепления на стенную поверхность в комплектации по запросу. Для ввода в эксплуатацию необходимо подвести трубопроводы: воду Ду 15 мм, канализацию – Ду 50 мм, вентиляцию – Ду – 50 мм. По ТЗ Заказчика возможна поставка с разной степенью автоматизации и в разной комплектации.
Принцип работы
В солерастворителе готовится насыщенный раствор поваренной соли с концентрацией до 300 г\л. Готовый насыщенный солевой раствор насосом-дозатором в требуемом количестве подается в тройник, одновременно туда же поступает вода, расход которой устанавливается ротаметром. Электролит требуемой концентрации подается в электролизер, где и происходит образование гипохлорита натрия с фиксированной концентрацией активного хлора. Готовый гипохлорит натрия сливается в накопительную емкость, откуда насосом-дозатором (или иным способом) забирается на обеззараживание. Водород, образовавшийся при электролизе водного раствора поваренной соли, разбавляется до взрывобезопасного состояния путем подачи воздуха через нагнетательный вентиллятор, и отводится из накопительной емкости за пределы электролизной. В процессе электролиза идет контроль тока электролиза, контроль наличия воздуха на разбавления водорода, контроль уровня гипохлорита в накопительной емкости.
Подробнее прочитать про принцип работы электролизных установок серии УЭ ГПХН можно по ссылке.
|
|
|
|
|
|
Комплектация
- Электролизер проточный
- Пульт управления с выпрямителем
- Резервуар гипохлорита натрия 200л
- Солерастворитель проточного типа 130 л
- Насос-дозатор раствора соли
- Насос-дозатор гипохлорита натрия
- Стабилизатор расхода воды
- Ротаметр
- Вентилятор напорный
- Системы трубопроводов с трубопроводной арматурой
- Система аварийных блокировок
- РамаДополнительно:
- Установка умягчения воды
- Контролер хлора с датчиками
- Контролер водорода с датчиками
- Водонагреватель
Возможна комплектация по требованию Заказчика или частичная комплектация.
Документы
Предоставляемые при поставке товара:
- Товарно-транспортная накладная
- Счет-фактура
- Акт приёма-передачи
- Документы либо их копии, подтверждающие соответствие товара требованиям, установленным в соответствии с действующим законодательством РФ (сан-эпидем заключение на установку, сан–эпидем заключение на ТУ)
- технический паспорт
- гарантийный талон
- руководство по эксплуатации на русском языке.
От 1 месяца. Поставщик должен согласовать с заказчиком дату (в случае досрочной поставки товара) и время поставки товара. Работаем по предоплате не менее 70%. Работаем без НДС. Отгрузка осуществляется после полной оплаты. При иных условиях изготовитель в праве изменить цену
электролизная установка .
| Электролизная Установка. |
|
|
|
||||||||||
| Электролизная установка GRUNDFOS Selcoperm |
|
|
|
||||||||||
| Лучшая электролизная установка на базе МБЭ пр-ва ГК СпецМаш ч.1 |
|
|
|
||||||||||
| Производство водорода |
|
|
|
||||||||||
| Электролизная установка “ЭльСоль” ЭУ-ПГН-001.006 |
|
|
|
||||||||||
| Электролизная установка NT-C-100. |
|
|
|
||||||||||
| ЭЛЕКТРОЛИЗНАЯ УСТАНОВКА ДЛЯ ЮВЕЛИРОВ |
|
|
|
||||||||||
| Сварка без баллонов! Газосварочный аппарат ЛИГА-02 Сварка и пайка без баллонов!Водородный аппарат |
|
|
|
||||||||||
| Монтаж электролизной установки Сиваш ЭГР 0100 |
|
|
|
||||||||||
| ПЕРЕВОДИМ Мотоцикл на водород – ВЗРЫВНОЙ эксперимент !!! |
|
|
|
||||||||||
| лига 02 c это наше всё)) |
|
|
|
||||||||||
| Электролизная вода от Гринлиф |
|
|
|
||||||||||
| Как собрать сварочный аппарат за 15 минут. Сварка на соляном растворе |
|
|
|
||||||||||
| Водородный генератор своими руками (HHO generator) |
|
|
|
||||||||||
| ГЕНЕРАТОР ВОДОРОДА ИЗ КИТАЯ! РЕЖЕМ МЕТАЛЛ ВОДОРОДОМ! ВОДОРОДНЫЙ РЕЗАК |
|
|
|
||||||||||
| Тест водородного сварочного аппарата “HHO BOX-8” Vol. 5 |
|
|
|
||||||||||
| Электролизёр на 50 пластин. Часть I – реактор. |
|
|
|
||||||||||
| Как сделать генератор водорода своими руками/How to make a DIY hydrogen generator |
|
|
|
||||||||||
| Электролизер генератор водорода первый опыт взрыв |
|
|
|
||||||||||
| ГЕНЕРАТОР ВОДОРОДА своими руками. Производит водород отдельно от кислорода. |
|
|
|
||||||||||
| Простейший электролизер своими руками |
|
|
|
||||||||||
| Электролизная установка типа Эль-Соль 2020 |
|
|
|
||||||||||
| Лучшая электролизная установка на базе МБЭ пр-ва ГК СпецМаш ч.2 |
|
|
|
||||||||||
| Разбор электролизера ЛИГА-02 |
|
|
|
||||||||||
| Лучшая электролизная установка на базе МБЭ пр-ва ГК СпецМаш ч.3 |
|
|
|
||||||||||
| Электролизная система отопления” rel=”spf-prefetch |
|
|
|
||||||||||
| STAR-1000 Отопление Водородом 20 батарей.” rel=”spf-prefetch |
|
|
|
||||||||||
| Электролизная установка” rel=”spf-prefetch |
|
|
|
||||||||||
| Как работает ячейка Мейера” rel=”spf-prefetch |
Электролиз воды
Если пропустить через воду электрический ток, жидкость начнёт диссоциироваться на составляющие молекулу воды атомы. В результате процесса электролиза воды получают кислород и водород. Однако в зависимости от природы электродов можно получить озон и перекись водорода.
Схема электролиза воды:
- анод:
2H2O → O2 + 4H+ + 4e–; - катод:
4H+ + 4e– → 2H2.
Или:
- анод:
3H2O → O3 + 6e– + 6H+; -
катод:
O2 + 2H2O + 2e– → H2O2 + 2OH–.
Общее уравнение:
2H2O → 2H2 + O2.
Рис. 2. Схема электролиза воды.
Вода – слабый электролит, поэтому электролиз чистой, дистиллированной воды протекает медленно или не идёт вовсе. Для ускорения процесса в воду добавляют сильный электролит, увеличивающий проводимость электрического тока.
Электролит выбирается так, чтобы исключить конкуренцию между катионами электролита и катионами воды (H+). В противном случае водород не будет произведён. Чтобы исключить конкуренцию, необходимо подобрать электролит, катионы которого будут иметь меньший электродный потенциал, чем H+ воды. На роль катиона электролита подходят:
- Li+;
- Rb+;
- K+;
- Cs+;
- Ba2+;
- Sr2+;
- Ca2+;
- Na+;
- Mg2+.
Для исключения конкуренции анионов, наоборот, подбирают электролит с анионами большего электродного потенциала, чем анион OH– воды. В качестве такого электролита применяется щелочь для образования гидроксильного иона OH–.
Рис. 3. Диссоциация щёлочи.
Для электролиза воды используются сильные щелочи: гидроксид калия (KOH) или натрия (NaOH). В некоторых случаях применяется сильная кислота, например, H2SO4.
Что мы узнали?
Электролиз – процесс образования и оседания на электродах ионов вещества под действием электрического тока. Вода разделяется на катионы водорода и анионы кислорода. Положительные катионы движутся к катоду, отрицательные анионы – к аноду. В некоторых случаях вода диссоциируется на озон и перекись водорода. Из-за низкой способности к диссоциации в воду добавляется сильный электролит, не мешающий образованию водорода и кислорода. Чаще всего добавляется щёлочь или сильная кислота.
Виды электролизеров
В зависимости от конструкции и принципа работы, различают электролизные установки 5 видов.
Сухие
Такие электролизеры состоят из пластинчатых электродов, разделенных между собой герметичными резиновыми прокладками. Часто «ячейки» установки дополнительно помещают в герметичный корпус.
Вырабатывающиеся в результате электролиза водород и кислород отводятся по специальным патрубкам, находящимся в торце корпуса или крайних пластин установки.
Проточные
Электролизные установки такого вида имеют следующее устройство:
- Электролизная ванна (корпус) с двумя патрубками, по одному из которых в нее подается электролит, по второму отводится образующийся в результате электролиза гремучий газ;
- Пластинчатые электроды, отделенные прокладками;
- Бак с электролитом, расположенный выше корпуса с электродами и соединенный шлангами с патрубками электролизной ванны установки и имеющий в верхней части патрубок с газовым клапаном.
При работе подобного устройства выделяющийся газ через патрубок и шланг попадает в бак с электролитом и, создавая в нем определенное давление, через клапан на отводном патрубке выходит за пределы установки.
Мембранные
Электролизные ячейки таких установок состоят из двух электродов, разделенных между собой тонкой мембраны, пропускающей продукты электролиза и разделяющей электроды между собой.
 Мембранная электролизная установка
Мембранная электролизная установка
Диафрагменные
Электролизные установки данного вида состоят из «U» образной колбы с двумя вставленными в нее электродами и 2-3 непроницаемыми диафрагмами. Используются подобные электролизеры для раздельного получения чистого водорода и кислорода.
Щелочные
В отличие от других моделей электролизеров, в таких в качестве электролита применяют раствор щелочи – каустическую соду (гидроксид натрия), являющийся не только дополнительным источником водорода и кислорода, но и катализатором для электролиза.
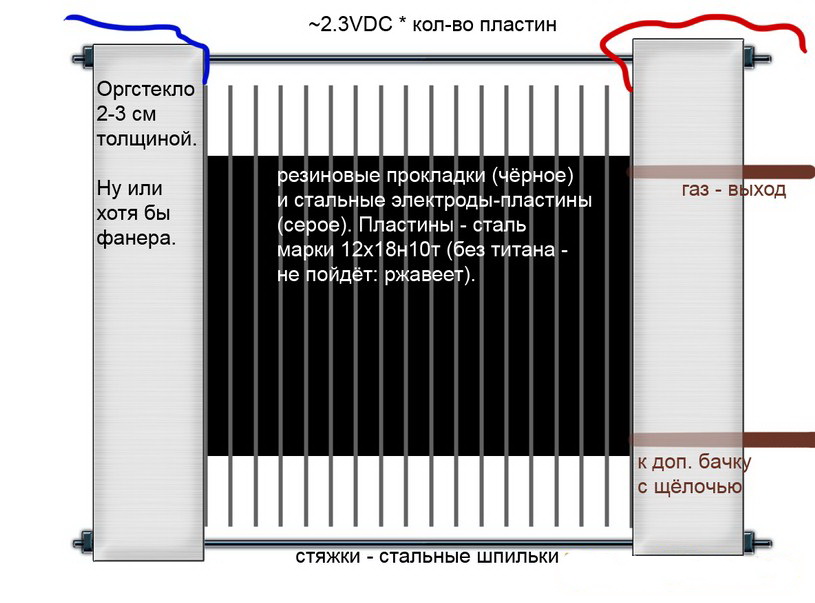 Схема щелочного электролизера
Схема щелочного электролизера
Такие установки, в отличие от аналогов других видов, позволяют применять более дешевые электроды из обычного железа.
Что такое электролизер, его характеристики и применение
Так называют устройство для одноименного электрохимического процесса, которому требуется внешний источник питания. Конструктивно это аппарат представляет собой заполненную электролитом ванну, в которую помещены два или более электродов.
Основная характеристика подобных устройств – производительность, часто это параметр указывается в наименовании модели, например, в стационарных электролизных установках СЭУ-10, СЭУ-20, СЭУ-40, МБЭ-125 (мембранные блочные электролизеры) и т.д. В данных случаях цифры указывают на выработку водорода (м3/ч).
 Промышленная стационарная электролизная установка, вырабатывающая 40 м3 водорода в час (СЭУ-40)
Промышленная стационарная электролизная установка, вырабатывающая 40 м3 водорода в час (СЭУ-40)
Что касается остальных характеристик, то они зависят от конкретного типа устройства и сферы применения, например, когда осуществляется электролиз воды, на КПД установки влияют следующие параметры:
- Уровень напряжения (минимального электродного потенциала), оно должно быть от 1,8 до 2 вольт, меньшее значение «не запустит» процесс, а большее приводит к чрезмерному расходу энергии, идущей на нагрев электролита. Если в качестве источника используется блок питания, например, на 14 вольт имеет смысл разделить емкость ванны пластинами на 7 ячеек, в соответствии с рисунком 2.
Таким образом, подавая на выходы 14 вольт, мы получим 2 вольта на каждой ячейке, при этом на пластинах с каждой стороны будут разные потенциалы. Электролизеры, где используется подобная система подключения пластин, называются сухими.
- Расстояние между пластинами (между катодным и анодным пространством), чем оно меньше, тем меньше будет сопротивление и, следовательно, больший ток пройдет через раствор электролита, что приведет к увеличению выработки газа.
- Размеры пластины (имеется в виду площадь электродов), прямо пропорциональны току, идущему через электролит, а значит, также оказывают влияние на производительность.
- Концентрация электролита и его тепловой баланс.
- Характеристики материала, используемого для изготовления электродов (золото – идеальный материал, но слишком дорогой, поэтому в самодельных схемах используется нержавейка).
- Применение катализаторов процесса и т.д.
Как уже упоминалось выше, установки данного типа могут использоваться как генератор водорода, для получения хлора, алюминия или других веществ. Они также применяются в качестве устройств, при помощи которых осуществляется очистка и обеззараживание воды (УПЭВ, VGE), а также проводится сравнительный анализ ее качества (Tesp 001).
 А) Установка прямого электролиза воды (УПЭВ); Б) анализатор качества воды Tesp 001
А) Установка прямого электролиза воды (УПЭВ); Б) анализатор качества воды Tesp 001
Нас, прежде всего, интересуют устройства, производящие газ Брауна (водород с кислородом), поскольку именно эта смесь имеет все перспективы для использования в качестве альтернативного энергоносителя или добавок к топливу. Их мы рассмотрим чуть позже, а пока перейдем к конструкции и принципу работы простейшего электролизера, расщепляющего воду на водород и кислород.
Проточные диафрагменные электрохимические реакторы с коаксиальными электродами
Четвертый этап ЭХА
| Элементы ПЭМ-1 и ПЭМ-3 | В 1989 г. были разработаны первые проточные электрохимические элементы ПЭМ, представляющие собой единичные элементы с коаксиально расположенными электродами, разделенными диафрагмой. Оптимальный выбор конструкции электролизеров и материалов определили дальнейшее развитие данного типа реакторов и показали элементы ПЭМ наиболее перспективными по сравнению с предыдущими типами реакторов. Начиная с 1990 г. технология развития ЭХА полностью базируется на использовании элементов ПЭМ, МБ (модулей Бахира) и реакторов на их основе. |
| Элементы МБ с диафрагмами ? 11 ммЭлементы МБ с диафрагмами ? 26-28 мм | В 2009 г. разработаны усовершенствованные типы элементов ПЭМ – элементы МБ или Модули Бахира. Элементы МБ являются универсальными и позволяют работать как с маломинерализованными, так и с концентрированными растворами. |
| В 2010 г. были выполнены работы по определению направлений дальнейшего совершенствования элементов МБ – существенному увеличению производительности элементов при одновременном упрощении их конструкции. | |
| Элементы МБ-100-01 и МБ-700-01 | В 2011 г. были созданы новые модели элементов МБ, обладающие повышенной производительностью, надежностью, долговечностью, хорошей ремонтопригодностью, способностью работать длительное время при повышенных нагрузках. Были найдены конструктивные и технологические решения, обеспечивающие возможность длительной работы элементов без ухудшения параметров на воде с большим содержанием солей жесткости, а также конструктивные и технологические решения, позволившие полностью отказаться от необходимости очистки катодных камер и диафрагмы элементов кислотой. |
Список источников
- www.asutpp.ru
- obrazovaka.ru
- amperof.ru
- www.specmach.ru
- vodorod-energy.ru
- vbinstitute.ru
- funer.ru
- www.rutteh.ru
- chemege.ru
 7 лестниц
7 лестниц 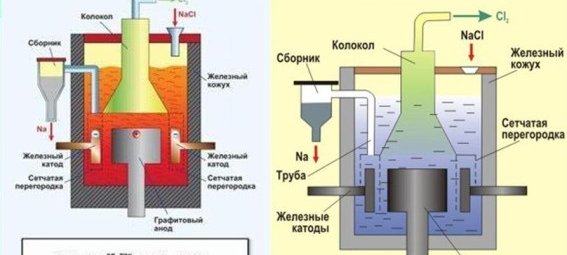




 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра
 Нажми для просмотра
Нажми для просмотра














